服务热线
400-611-2850
百替医学是国内首家专注于医学科研咨询及技术服务的公司,专门为临床医生提供科研问题解决方案。
Phone: 400-611-2850
E-mail:: service@100biotech.com
或 在线留言 给我们
1、联系与咨询。
您可通过公司的服务热线400-611-2850和服务邮箱 service@100biotech.com,或者与您联系的百替医学服务人员,告知您的科研服务需求2、签订保密协议,洽谈具体服务内容。
在双方签订合作保密协议后,您可与百替医学科研服务咨询小组进行具体项目沟通;您和百替医学双方明确服务产品需求和具体项目要求;百替医学制作和提交项目实施方案和报价。3、双方签订合同,客户按合同支付费用。
双方对合同服务内容和价格无异议后,签订服务合同。您按合同约定支付费用,并提供必要的实验药品或样品(实验样品的寄送须采用特快专递形式邮寄,有低温要求的、固定要求的,按低温保存、固定防碎方法运输,以确保安全可靠)。4、项目实施,开始为客户提供科研咨询和技术服务。
百替医学按合同方案进行项目实施。项目实施过程中,百替医学项目经理按时与客户反馈及交流信息;百替医学开始为客户提供相关科研咨询和技术服务,并及时按合同将数据、材料、样本、模型等相关信息材料提供给客户。5、分析结果资料,整理提交数据。
百替医学技术团队分析整理数据,总结结论,将完整项目实施报告和数据、图片等相关信息提供给客户,同时根据合同处理相关的实验材料。项目报告内容将包括具体实验方法、步骤、所用试剂、仪器、数据、结果和结论等。6、项目完成,协商进一步合作。
项目完成,客户如有后续科研服务需求,双方协商进一步合作。

癌-星形胶质细胞间隙连接通过cGAMP转运促进脑转移瘤发展
发布时间:2016-05-25 16:23 文章来源:未知 作者:百替生物
脑转移瘤系指原发于身体其他部位的肿瘤细胞转入颅内,其中以肺癌脑转移最常见。在许多恶性程度高的肿瘤中,发现有20%-40%发生脑转移。目前针对脑转移瘤尚缺乏有效的治疗策略,许多患者发生脑转移瘤后不到12个月,即死亡。因此,急需研究开发出更好的治疗策略。
近几年,关于脑转移瘤的分子以及细胞机制得到了一定的阐释:循环肿瘤细胞首先通过血脑屏障(blood–brain barrier, BBB)进入软细胞组织。许多进入软细胞组织的肿瘤细胞被星形胶质细胞消灭。星形胶质细胞在中枢神经系统中发挥营养、保护作用,大概就是这样的——
作者研究发现在脑转移瘤中,存在较高的Cx43的表达,对比脑转移瘤、原发肿瘤和正常组织,也观察到脑转移瘤中高水平的Cx43,Cx43是间隙连接组成的分子。为了更好的观察癌细胞-星形胶质细胞的联系,作者运用了5个来源于人和小鼠的脑转移瘤模型:乳腺癌(MDA231-BrM2和ErbB2-BrM),肺癌(H2030-BrM3, 393N1和LLC-BrM)。细致观察发现Cx43表达在癌细胞-星形胶质细胞接触处,在星形胶质细胞中表达最高,PCDH7在乳腺癌和肺癌中高表达,同时在脑转移瘤中,PCDH7水平较高,而且在脑转移癌细胞中的含量高于星形胶质细胞、小胶质细胞或内皮细胞。在临床三阴乳腺癌(triple-negative breast cancer, TNBC)中,发现原发肿瘤中Cx43和PCDH7的含量与脑转移有关,而不是骨转移或者肺转移。在非小细胞肺癌(non-small cell lung cancer, NSCLC)也观察到同样的现象。这些证据表明Cx43主要表达与星形胶质细胞,PCDH7主要表达与癌细胞,Cx43和PCDH7与脑转移瘤相关。
预先将染料导入癌细胞中,抑制Cx43和PCDH7的表达,抑制了染料进入星形胶质细胞,表明Cx43和PCDH7均与细胞间间隙连接有关。在大脑中,内皮细胞和小胶质细胞不表达或低表达Cx43和PCDH7,也很少观察到有染料进入这些细胞,因此,在大脑中,PCDH7主要介导癌细胞与星形胶质细胞的联系。为了进一步论证Cx43与PCDH7的关系,以及其在间隙连接形成中的作用,采用荧光素酶实验,分别将荧光素酶的N端和C端与PCDH7和Cx43进行连接,进行不同分组实验证明,PCDH7与Cx43存在相互作用,PCDH7促进了Cx43形成间隙连接的能力。体内实验研究发现,干扰PCDH7或者Cx43的表达,抑制了大脑中癌细胞的存在,体外划痕实验证实,PCDH7或者Cx43的表达下降,癌细胞细胞的增殖能力也显著减弱。这充分表明PCDH7促进Cx43形成间隙连接,在脑转移瘤的发展中发挥促进作用。
然而PCDH7促进Cx43形成间隙连接,增强脑转移瘤的发展的机制如何,尚不明确。通过TRAPRNA-seq分析发现,Cx43下调的情况下,癌细胞中IFN和NF-kB通路分子表达降低。癌细胞-星形胶质细胞共培养,促进癌细胞中SIRT1和NF-kB p65蛋白磷酸化,表明激活了癌细胞中IFN和NF-kB通路,同时星形胶质细胞中STING通路下游炎症细胞因子IFNα和TNF水平增加。体内实验抑制癌细胞中SIRT1,大脑中转移癌细胞显著减少。这些表明Cx43形成的间隙连接促进星形胶质细胞IFNα和TNF产生,激活癌细胞SIRT1和NF-kB通路。
IFNα和TNF的上升与细胞中dsRNA相关,细胞质中dsRNA激活cGAS-STING通路,启动抗病毒免疫反应,这个过程是通过第二信使cGAMP介导的。cGAMP结合STING触发TBK1和IRF3的磷酸化导致其激活,激活的IRF3进入细胞核,促进IFNα和TNF表达。体外共培养癌细胞-星形胶质细胞,发现TBK1和IRF3的磷酸化与Cx43的表达正相关,IRF3在细胞核中聚集只在星形胶质细胞中发现。同时研究发现,抑制STING,并不能观察到IRF3的核聚集现象,IFNα和TNF表达也不会上升。这表明Cx43和STING通路与IRF3的核聚集以及IFNα和TNF表达相关。为了进一步明确在脑转移瘤中STING的激活是否与dsRNA下游的cGAMP有关,通过液相色谱串联质谱分析发现cGAMP产生于癌细胞中,进入星形胶质细胞,抑制Cx43的表达,星形胶质细胞中cGAMP的水平下降。这些结果表明,脑转移癌细胞中产生的cGAMP通过Cx43组装成的间隙连接进入星形胶质细胞,集合STING,出发IRF3的磷酸化,并进入细胞核,促进IFNα和TNF表达。
运用间隙连接调节因子甲氯芬那酸和tonabersat,抑制间隙连接的组装,观察到星形胶质细胞中IFNα和TNF的表达下降,且存在剂量依赖性。体内实验也证实,运用甲氯芬那酸和tonabersat处理,脑转移瘤发展得到显著抑制,与Cx43和PCDH7的敲除相类似。这些体内体外实验结果表明,间隙连接抑制剂甲氯芬那酸和tonabersat具有显著的抑制脑转移瘤发展的作用。
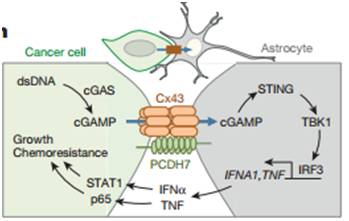
这篇研究论文丰富了癌细胞-星形胶质细胞在脑转移瘤发展中的作用,阐明了两者之间的间隙连接在脑转移瘤发展中的作用,进一步运用药物处理的实验表明以癌细胞-星形胶质细胞之间间隙连接作为靶点,是一个可靠、有效的治疗脑转移瘤的策略,具有重大的科学意义和应用前景。